
அனைத்து iLive உள்ளடக்கம் மருத்துவ ரீதியாக மதிப்பாய்வு செய்யப்படும் அல்லது முடிந்தவரை உண்மையான துல்லியத்தை உறுதி செய்ய உண்மையில் சரிபார்க்கப்படுகிறது.
நாம் கடுமையான ஆதார வழிகாட்டுதல்களை கொண்டிருக்கிறோம் மற்றும் மரியாதைக்குரிய ஊடக தளங்கள், கல்வி ஆராய்ச்சி நிறுவனங்கள் மற்றும் சாத்தியமான போதெல்லாம், மருத்துவ ரீதியாக மதிப்பாய்வு செய்யப்பட்ட படிப்புகளை மட்டுமே இணைக்கிறோம். அடைப்புக்களில் உள்ள எண்கள் ([1], [2], முதலியன) இந்த ஆய்வுகள் தொடர்பான கிளிக் செய்யக்கூடியவை என்பதை நினைவில் கொள்க.
எங்கள் உள்ளடக்கத்தில் எதையாவது தவறாக, காலதாமதமாக அல்லது சந்தேகத்திற்குரியதாகக் கருதினால், தயவுசெய்து அதைத் தேர்ந்தெடுத்து Ctrl + Enter ஐ அழுத்தவும்.
புதிய அணுகுமுறை புற்றுநோய் உயிரணு தழுவலைத் தடுக்கிறது மற்றும் கீமோதெரபியின் செயல்திறனை இரட்டிப்பாக்குகிறது
கடைசியாக மதிப்பாய்வு செய்யப்பட்டது: 27.07.2025
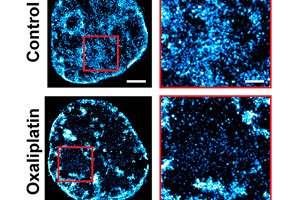
புற்றுநோய் சிகிச்சைக்கு முற்றிலும் புதிய அணுகுமுறையில், நார்த்வெஸ்டர்ன் பல்கலைக்கழகத்தைச் சேர்ந்த உயிரி மருத்துவப் பொறியாளர்கள், விலங்கு பரிசோதனையில் கீமோதெரபியின் செயல்திறனை இரட்டிப்பாக்கியுள்ளனர்.
புற்றுநோயை நேரடியாகத் தாக்குவதற்குப் பதிலாக, இந்த தனித்துவமான உத்தி புற்றுநோய் செல்கள் சிகிச்சைகளுக்கு எதிர்ப்புத் திறன் கொண்டதாக மாறுவதைத் தடுக்கிறது - இது ஏற்கனவே உள்ள மருந்துகளுக்கு நோயை அதிக எளிதில் பாதிக்கக்கூடியதாக ஆக்குகிறது. இந்த அணுகுமுறை செல் கலாச்சாரங்களில் நோயை கிட்டத்தட்ட ஒழித்தது மட்டுமல்லாமல், கருப்பை புற்றுநோயின் எலி மாதிரிகளில் கீமோதெரபியின் செயல்திறனையும் கணிசமாக மேம்படுத்தியுள்ளது.
இந்த ஆய்வு தேசிய அறிவியல் அகாடமியின் செயல்முறைகள் இதழில் வெளியிடப்பட்டது.
"புற்றுநோய் செல்கள் சிறந்த தகவமைப்புகள்" என்று ஆய்வுக்கு தலைமை தாங்கிய நார்த்வெஸ்டர்ன் பல்கலைக்கழகத்தைச் சேர்ந்த வாடிம் பேக்மேன் கூறுகிறார். "அவை கிட்டத்தட்ட எதற்கும் தகவமைத்துக் கொள்ள முடியும். முதலில், அவை நோயெதிர்ப்பு மண்டலத்தைத் தவிர்ப்பது எப்படி என்பதைக் கற்றுக்கொள்கின்றன. பின்னர் கீமோதெரபி, நோயெதிர்ப்பு சிகிச்சை மற்றும் கதிர்வீச்சை எவ்வாறு எதிர்ப்பது என்பதைக் கற்றுக்கொள்கின்றன. இந்த சிகிச்சைகளுக்கு அவை எதிர்ப்புத் திறன் கொண்டதாக மாறும்போது, அவை நீண்ட காலம் வாழ்கின்றன, மேலும் புதிய பிறழ்வுகளைப் பெறுகின்றன. புற்றுநோய் செல்களை நேரடியாகக் கொல்ல நாங்கள் விரும்பவில்லை. அவற்றின் வல்லமையை - தகவமைத்துக் கொள்ள, மாற்ற, மற்றும் தவிர்க்க அவற்றின் உள்ளார்ந்த திறனை - பறிக்க விரும்பினோம்."
பேக்மேன், நார்த்வெஸ்டர்ன் பல்கலைக்கழகத்தின் மெக்கார்மிக் பொறியியல் பள்ளியில் சாக்ஸ் குடும்ப உயிரி மருத்துவ பொறியியல் மற்றும் மருத்துவப் பேராசிரியராக உள்ளார், அங்கு அவர் இயற்பியல் மரபியல் மற்றும் பொறியியல் மையத்தை இயக்குகிறார். அவர் ராபர்ட் எச். லூரி விரிவான புற்றுநோய் மையம், வாழ்க்கை செயல்முறைகளின் வேதியியல் நிறுவனம் மற்றும் சர்வதேச நானோ அறிவியல் நிறுவனம் ஆகியவற்றின் உறுப்பினராகவும் உள்ளார்.
புற்றுநோய் உயிர்வாழ்வதற்கான திறவுகோல் குரோமாடின் ஆகும்.
புற்றுநோய்க்கு பல தனித்துவமான அம்சங்கள் உள்ளன, ஆனால் அவை அனைத்திற்கும் அடிப்படையாக ஒரு பண்பு உள்ளது: அதன் இடைவிடாத உயிர்வாழும் திறன். நோயெதிர்ப்பு அமைப்பு மற்றும் தீவிரமான மருத்துவ சிகிச்சைகள் ஒரு கட்டியைத் தாக்கினாலும், புற்றுநோய் சுருங்கலாம் அல்லது வளர்ச்சியில் மெதுவாக இருக்கலாம், ஆனால் அது அரிதாகவே முற்றிலும் மறைந்துவிடும். மரபணு மாற்றங்கள் எதிர்ப்புத் திறனுக்கு பங்களித்தாலும், மன அழுத்தத்திற்கு புற்றுநோய் செல்கள் விரைவாக பதிலளிப்பதைக் கணக்கிட முடியாத அளவுக்கு பிறழ்வுகள் மிக மெதுவாக நிகழ்கின்றன.
தொடர்ச்சியான ஆய்வுகளில், பேக்மேனின் குழு இந்தத் திறனை விளக்கும் ஒரு அடிப்படை வழிமுறையைக் கண்டுபிடித்தது. குரோமாடின் எனப்படும் மரபணுப் பொருளின் சிக்கலான அமைப்பு, மிகவும் சக்திவாய்ந்த மருந்துகளைக் கூட மாற்றியமைத்து உயிர்வாழும் புற்றுநோயின் திறனைத் தீர்மானிக்கிறது.
டி.என்.ஏ, ஆர்.என்.ஏ மற்றும் புரதங்கள் உள்ளிட்ட பெரிய மூலக்கூறுகளின் குழுவான குரோமாடின், எந்த மரபணுக்கள் அடக்கப்படுகின்றன, எவை வெளிப்படுத்தப்படுகின்றன என்பதை தீர்மானிக்கிறது. மரபணுவை உருவாக்கும் இரண்டு மீட்டர் டி.என்.ஏவை செல்லின் கருவில் நூறில் ஒரு பங்கு மில்லிமீட்டரில் ஒரு இடத்தில் அடைக்க, குரோமாடின் மிகவும் சுருக்கப்பட்டுள்ளது.
இமேஜிங், மாடலிங், சிஸ்டம்ஸ் பகுப்பாய்வு மற்றும் இன் விவோ பரிசோதனைகளை இணைப்பதன் மூலம், இந்த தொகுப்பின் 3D கட்டமைப்பு எந்த மரபணுக்கள் செயல்படுத்தப்படுகின்றன மற்றும் செல்கள் மன அழுத்தத்திற்கு எவ்வாறு பதிலளிக்கின்றன என்பதைக் கட்டுப்படுத்துவது மட்டுமல்லாமல், மரபணு டிரான்ஸ்கிரிப்ஷன் வடிவங்களின் "நினைவகத்தை" தொகுப்பு வடிவவியலில் உடல் ரீதியாக குறியாக்கம் செய்ய செல்களை அனுமதிக்கிறது என்பதை பேக்மேனின் குழு கண்டறிந்தது.
மரபணுவின் முப்பரிமாண அமைப்பு, இயந்திர கற்றல் வழிமுறையைப் போலவே, சுய-கற்றல் அமைப்பாகச் செயல்படுகிறது. அது "கற்றுக்கொள்ளும்போது", இந்த ஏற்பாடு தொடர்ந்து ஆயிரக்கணக்கான நானோஸ்கோபிக் குரோமாடின் பேக்கிங் டொமைன்களாக மறுசீரமைக்கப்படுகிறது. ஒவ்வொரு டொமைனும் செல்லின் டிரான்ஸ்கிரிப்ஷனல் நினைவகத்தின் ஒரு பகுதியைச் சேமிக்கிறது, இது செல் எவ்வாறு செயல்படுகிறது என்பதைத் தீர்மானிக்கிறது.
கீமோதெரபியை மேம்படுத்த குரோமாடினை மறுநிரலாக்கம் செய்தல்
புதிய ஆய்வில், பேக்மேனும் அவரது சகாக்களும் ஒரு கணக்கீட்டு மாதிரியை உருவாக்கினர், இது குரோமாடின் பேக்கிங் புற்றுநோய் செல்லின் கீமோதெரபியில் உயிர்வாழும் வாய்ப்பை எவ்வாறு பாதிக்கிறது என்பதை பகுப்பாய்வு செய்ய இயற்பியல் கொள்கைகளைப் பயன்படுத்துகிறது. பல்வேறு வகையான புற்றுநோய் செல்கள் மற்றும் கீமோதெரபி மருந்துகளின் வகைகளுக்கு மாதிரியைப் பயன்படுத்துவதன் மூலம், சிகிச்சை தொடங்குவதற்கு முன்பே - செல் உயிர்வாழ்வை துல்லியமாக கணிக்க முடியும் என்று குழு கண்டறிந்தது.
புற்றுநோய் செல் உயிர்வாழ்வதற்கு குரோமாடின் பேக்கேஜிங் மிக முக்கியமானதாக இருப்பதால், விஞ்ஞானிகள் தங்களைத் தாங்களே கேட்டுக்கொண்டனர்: பேக்கேஜிங் கட்டமைப்பை மாற்றினால் என்ன நடக்கும்? புதிய மருந்துகளை உருவாக்குவதற்குப் பதிலாக, செல் கருக்களுக்குள் உள்ள இயற்பியல் சூழலை மாற்றியமைக்கக்கூடிய மற்றும் குரோமாடின் பேக்கேஜிங்கை பாதிக்கக்கூடிய வேட்பாளர்களைக் கண்டறிய, நூற்றுக்கணக்கான மருந்துகளை அவர்கள் திரையிட்டனர்.
இறுதியில், குழு, மூட்டுவலி மற்றும் இருதய நோய்களுக்கு சிகிச்சையளிக்க ஏற்கனவே பயன்படுத்தப்படும் FDA-அங்கீகரிக்கப்பட்ட அழற்சி எதிர்ப்பு மருந்தான செலிகோக்சிப்பைத் தேர்ந்தெடுத்தது, மேலும் இது ஒரு பக்க விளைவாக, குரோமாடினின் பேக்கேஜிங்கை மாற்றுகிறது.
பரிசோதனை முடிவுகள்
நிலையான கீமோதெரபியுடன் செலிகாக்சிப்பை இணைப்பதன் மூலம், இறந்த புற்றுநோய் செல்களின் எண்ணிக்கையில் குறிப்பிடத்தக்க அதிகரிப்பை ஆராய்ச்சியாளர்கள் கண்டனர்.
கருப்பை புற்றுநோயின் எலி மாதிரிகளில், பக்லிடாக்சல் (ஒரு பொதுவான கீமோதெரபி மருந்து) மற்றும் செலிகாக்சிப் ஆகியவற்றின் கலவையானது புற்றுநோய் செல் தழுவல் விகிதத்தைக் குறைத்து, கட்டி வளர்ச்சி அடக்கலை மேம்படுத்தி, பக்லிடாக்சலின் விளைவை மட்டும் விஞ்சியது.
"நாங்கள் குறைந்த அளவிலான கீமோதெரபியைப் பயன்படுத்தியபோது, கட்டிகள் தொடர்ந்து வளர்ந்தன. ஆனால் கீமோதெரபியில் ஒரு வேட்பாளர் TPR (டிரான்ஸ்கிரிப்ஷனல் பிளாஸ்டிசிட்டி ரெகுலேட்டர்) ஐச் சேர்த்தவுடன், மிகவும் குறிப்பிடத்தக்க வளர்ச்சித் தடுப்பைக் கண்டோம். இது செயல்திறனை இரட்டிப்பாக்கியது," என்று பேக்மேன் கூறினார்.
சாத்தியமான வாய்ப்புகள்
இந்த உத்தி மருத்துவர்கள் குறைந்த அளவிலான கீமோதெரபியைப் பயன்படுத்த அனுமதிக்கும், இதனால் கடுமையான பக்க விளைவுகள் குறையும். இது நோயாளியின் வசதியையும் புற்றுநோய் சிகிச்சையின் அனுபவத்தையும் கணிசமாக மேம்படுத்தும்.
இருதய மற்றும் நரம்புச் சிதைவு நோய்கள் உள்ளிட்ட பிற சிக்கலான நோய்களுக்கு சிகிச்சையளிப்பதில் குரோமாடினை மறுநிரலாக்கம் செய்வது முக்கியமாக இருக்கும் என்று பேக்மேன் நம்புகிறார்.
